jueves, 13 de diciembre de 2012
domingo, 25 de noviembre de 2012
sábado, 24 de noviembre de 2012
Nuevo inquilino en el Laboratorio
Ayer, día 23 de noviembre recibimos a la nueva mascota, previamente bautizada como ''Benceno'' y posteriormente como ''Rutherford-Benceno'', un inquieto hámster con el que realizaremos algunos experimentos.
Paula Urbina
martes, 20 de noviembre de 2012
viernes, 2 de noviembre de 2012
Espejo de plata
El proceso consistía en:
-Echar la disolución de nitrato de plata seguido de un par de gotas de sosa que diese lugar a la formación un precipitado negro.
-Después tuvimos que echar "unas"gotas de amoniaco aunque a causa de su concentración se convirtieron en alguna más de la cuenta, agitando hasta hacer desaparecer el precipitado negro.
-Una vez que nuestra disolución se volvía trasparente, se le echaría la disolución de glucosa en tanta cantidad como volumen de líquido tuviese el tubo de ensayo.
-Por último nuestras disoluciones se podrían al baño maría para conseguir obtener(en algunos casos) un bonito espejo de plata que rodease nuestro tubo de ensayo.
Los afortunados que realizaron bien la práctica tendrán en sus casas esta muestra de espejo de plata(a no ser que se les haya roto de camino a casa).

Esta es una imagen (tomada de las prácticas del año pasado, ya que no sacamos fotos del proceso) donde se representa el proceso de formación del espejo de plata en las paredes del tubo de ensayo.
Sara y Cecilia
Epidermis de cebolla
Hace unas semanas realizamos ya nuestras primeras prácticas, una de ellas fue la observación de una epidermis de cebolla al microscopio.
Los pasos realizados fueron los siguientes:
-Separamos las capas de la cebolla hasta poder extraer una muestra lo suficientemente fina como para trabajar con ella.
-Colocamos la muestra sobre el portaobjetos (situado sobre el vaso de precipitados) y añadimos agua sobre la muestra.
-Escurrimos el agua y añadimos unas gotas de azul de metileno sobre la muestra.
-Tras esperar 10 minutos, bañamos la epidermis con agua para que desprendiese el colorante.
-Finalmente la muestra ya estaba lista para ser observada al microscopio y tomar imágenes de la muestra.
En esta muestra se puede observar las células de la cebolla vistas al microscopio, diferenciando los núcleos. Esta fue nuestra segunda imagen tomada ya que en la primera había partes de la muestra en la que se veían las células superpuestas.
Cecilia
lunes, 23 de abril de 2012
Limpieza en el laboratorio
Guión de la Práctica
Objetivo de la Práctica
Dejar nuestro habitáculo como los chorros del oro, para el uso y disfrute de nuestros sucesores.Fundamento de la práctica
DAR CERA, PULIR CERAMateriales y reactivos:
Reactivos:- 24 escolares a punto de ser mayores de edad, a ser posible no muy hormonados (que los hombres sudamos).
- Fairy
- H2O
- Escoba
- Fregona
- Cubo
- Espuma sobrante (aun se deben 50€ a @pabloinfiesta)
- Bolsas de basura
Procedimiento experimental
Aplicar el fundamento de la práctica a base de bien. Llegar a cada recoveco y no dejarse nada por vagancia. Objetivo secundario: abrir la puerta del armario de metal. REcoger el peachímetro a ser posible, y los modelos moleculares también, que pasan frío (@JValdes117 lo agradecerá).Cálculos a realizar
Cantidad de fairy: Basta con coger una gota, que eso dice el anuncio.Valoración del pH de la pintura con agua hasta que desaparezca todo rastro de pintura.
Opinión personal
Duro trabajo realmente, seguimos sudando, pero por ser hombres, ya que estamos escribiendo esta humilde memoria mientras nuestros compañer@s lo limpian con el sudor (sí, otra vez) de su frente.Muchas gracias!
Álvaro de Vicente Blanco (lo que queda de Calamardo), Enol Álvarez Molinuevo (Bob en horas bajas) y Pablo Infiesta de la Roza (Patricio)
sábado, 31 de marzo de 2012
La práctica más escurridiza
1. Introduce el pez en la cubeta de disección y obsérvalo detenidamente tratando de reconocer las partes más importantes de su anatomía externa.
ORGANOGRAFÍA INTERNA
Una vez realizada esta disección, observaremos la cavidad visceral al descubierto.
jueves, 29 de marzo de 2012
Huelga en el lab
El trabajo de hoy ha sido como quien dice algo simplón. Sólo unos pocos entramos para repetir la valoración de NaOH con HCl. Los valores que nos había dado para el NaOH el otro día pensábamos que no eran los correctos,pero repentinamente surgió un bote con el mismo número pero con distinta M...Cosas que pasan.
Bueno, aquí os dejamos hasta después de estas vacaciones.
Felices Pascuas
Pablo Infiesta, Pañeda y Enol
miércoles, 21 de marzo de 2012
Valoración del pH del vinagre
Con unos 10 ml de vinagre, que habiamos colocado en un Erlenmeyer, a los que se le habia echado 2 gotas de fenolftaleina (que vira entre el 8 y el 9 de alcalinidad), poco a poco, gota a gota, golpe a golpe, verso a verso... Fuimos virtiendo disolución de NaOH O.5M comprobando asi, el grado de acidez el vinagre (se podia observar un cambio de color).
En la proxima entrada, se añadiran unas fotos y un video donde podreis observar el momento justo donde vira la fenolftaleina apocaliptamente.
Un abrazo.
PPPI (Pañeda Infiesta)
viernes, 16 de marzo de 2012
Té de lombarda

- Ácido sulfúrico: color rojo.
- Ácido cítrico: rosa con fibras en suspensión.
- Amoníaco: verde con tonalidad amarilla en la parte inferior del tubo.
- Ácido clorhídrico: rosa muy fuerte.
- Vinagre: color indefinido de tonalidad amarillenta y con precipitado en el fondo.
- Carbonato de sodio: tonalidad verdosa, semejante al jade.

jueves, 15 de marzo de 2012
Indicadores de pH
El color original del líquido era el de la imagen que aparece a continuación:

sábado, 10 de marzo de 2012
Mitosis en células de raíz de cebolla
En primer lugar, y después de tener unos días la cebolla en agua con el fin de que las raíces creciesen, cortamos parte del extremo final de la raíz, ya que esa es la zona donde las células se encuentran en división.
A continuación colocamos las muestras que habíamos cortado en un vidrio de reloj y añadimos orceína A. Para que esta tinción tuviese efecto sobre las raíces, había que calentar el vidrio durante 8 minutos, teniendo en cuenta que, en el momento en el que se produjesen vapores fuertes, había que retirar la muestra.
Tras este paso, colocamos una de las raíces sobre un portaobjetos y añadimos orceína B dejándola actuar aproximadamente durante 1 minuto.
Como paso final, colocamos un cubreobjetos sobre la muestra y con la ayuda de un papel retiramos el tinte sobrante y de esta manera, ya teníamos nuestra nuestra preparada para observar al microscopio.
Tras varios días tratando de detectar en las células las distintas fases de la mitosis celular, finalmente mi compañera y yo logramos encontrarlas y aquí os mostramos las imágenes:
PROFASE


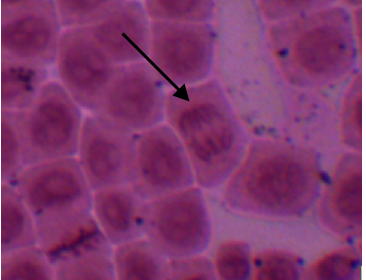
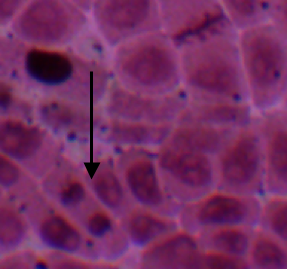
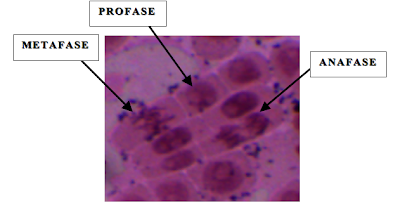
miércoles, 29 de febrero de 2012
viernes, 24 de febrero de 2012
PRÁCTICA DEL EQUILIBRIO QUÍMICO I
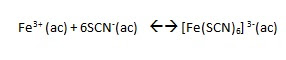
El tubo 1 lo dejamos como "control" al haber echado 1 ml de una disolución de cloruro de hierro y 1 ml de tiocianato potásico y 50 ml de agua, quedando un color rojizo.
En el tubo 2, a parte de la disolución anterior añadimos disolución de tiocianato potásico (KSCN), quedando un color rojo, puesto quen al aumentar la cantidad de SCN, el equilibrio se desplazaba hacia la derecha.
En el tubo 3, añadimos a la disolución control, hidróxido de sodio (NaOH) reaccionando con el ión hierro y produciendo el hidróxido de hierro, por tanto se forma un precipitado. El contenido del tubo 3 lo dividimos en dos tubos, uno que lo dejamos como testigo y otro lo añadimos HCl para que desaparezca ese precipitado (lo podemos observar en el tubo 6)
En el tubo 4, añadimos a la disolución inicial control NaI; y el color amarillo señala que el color está desplazado hacia la izquierda.
Por último, añadimos en el tubo 5, tricloruro de hierro; y al aumentar la cantidad de iones hierro la reacción se desplaza hacia la derecha para gastar esos reactivos, y se muestra el color rojizo de la disolución
Atentamente, Sara y Deva
miércoles, 22 de febrero de 2012
INFLUENCIA DE LA TEMPERATURA EN EL DESPLAZAMIENTO DEL EQUILIBRIO QUÍMICO (2ª parte)
INFLUENCIA DE LA TEMPERATURA EN EL DESPLAZAMIENTO DEL EQUILIBRIO QUIMICO
viernes, 17 de febrero de 2012
¡Habemus minioricios!

Obtuvimos las siguientes fotos que corresponden al desarrolo temprano del oricio:



sábado, 11 de febrero de 2012
Gran experiencia en el laboratorio
Para familiarizarnos con nuestro nuevo compañero, comenzamos observando su aspecto exterior y tratamos de detectar todas las entradas y salidas. Colocamos el corazón en la cubeta de disección de manera que la cara más plana quedase hacia arriba. A continuación, intentamos detectar todas las venas y arterias que salían y entraban, lo cual no fue tarea fácil, sin embargo lo conseguimos y aquí os las mostramos.

La sangre que bombea el corazón, realiza dos circuitos diferentes, antes de volver a él:
- Circulación mayor: Comienza en el ventrículo izquierdo, la sangre atraviesa la válvula aórticay la sangre cargada de oxígeno sale por la arteria aorta hacia el sistema capilar. Allí las arterias se transforman en venas que contienen los productos de desecho, como el co2 de las células y es una sangre pobre en oxígeno. Esta sangre llega de nuevo al corazón a través de las venas cava, superior e inferior que desembocan en la aurícula derecha y pasa al ventrículo derecho a través de la válvula tricúspide, donde comenzará la circulación menor.
- Circulación menor: Este circuito comienza en el ventrículo derecho donde la sangre pobre en oxígeno atraviesa la válvula pulmonar para, a través de las arterias pulmonates, llegar a los pulmones donde se hará un intercambio entre los productosde desecho y el oxígeno de manera que se obtiene sangre rica en oxígeno, la cual, a través de las venas pulmonares, llega a la aurícula izquierda . Allí atraviesa la válvula mitral y pasa al ventrículo izquierdo donde comienza, de nuevo, la circulación mayor.
]
El garbanzo y la bureta
A día de hoy, en nuestra mesa de trabajo, el garbanzo aún se encuentra en la bureta, pero ahora está inmerso en ácido sulfúrico. Explicaremos el porqué:
-El ácido sulfúrico, de fórmula H2SO4, a temperatura ambiente es un líquido corrosivo, es más pesado que el agua e incoloro (a temperatura y presión ambiente).
- Este compuesto es soluble en agua, pero reacciona violentamente al mezclarse con ella, generando calor.
- Éste es un ácido fuerte, es decir, en disolución acuosa se disocia fácilmente en iones de hidrógeno (H+) e iones sulfato (SO42-)
jueves, 9 de febrero de 2012
El Patatómetro: Vol. 1
- Tanto la arteria aorta como la vena cava son las más gruesas (circulación mayor, es decir, a lo largo de todo el cuerpo)
- El ventrículo izquierdo presenta una pared muscular más gruesa, ya que es el encargado de impulsar la sangre a todo el cuerpo
- Aproximadamente el corazón late más de 30 millones de veces al año
- Los glóbulos rojos viven una media de 4 meses y realizan unas 172.000 vueltas alrededor del cuerpo
- El primer trasplante de corazón fue realizado en el año 1967
Corazones rotos
Y esto es lo que Lucía y Eva os cuentan.
martes, 7 de febrero de 2012
Tortuga misteriosa
lunes, 6 de febrero de 2012
El secreto de la tortuga "Chelonia"
(El sello en sí no se ve muy bien, pero en la realidad es parecido...)
Las curiosas Laura García Coto y Lucía Menéndez Rodríguez.
miércoles, 1 de febrero de 2012
Curiosidades
martes, 31 de enero de 2012
Funcionamiento del corazón
Tras realizar un pequeño trabajo de investigación sobre sus partes y funcionamiento, mañana pondremos a prueba nuestros conocimientos con la "mítica" maqueta del corazón que ha pasado numerosas veces por nuestras manos en cursos anteriores. Pero este año hay una diferencia: haremos frente a uno de verdad.
Así que, para sacarle el máximo partido a esta experiencia, aquí os dejamos un vídeo de repaso para "refrescar" algunos conceptos básicos sobre su funcionamiento.
Juncal e Inés.
miércoles, 25 de enero de 2012
Semana sin Valdés
Un saludete de parte de: Deva, Sara, María Pumares y Alonso y Lucía García.
viernes, 20 de enero de 2012
Pequeños agricultores: primera toma de contacto
Por ahora los resultados no son los mejores. Sin embargo nuestro equipo no pierde las esperanzas de ver crecer el producto de lo que con tanto amor hemos sembrado.
Además no podemos olvidar que en el mundo de la ciencia los mayores avances sólo aparecen tras una época de sequía (nunca mejor dicho) de resultados.
De momento todo el equipo está comprometido con la causa y hemos organizado turnos para asegurarnos de que a nuestras "criaturas" no les falte de nada.
El otro día tuvimos un "problemilla" ya que nos quedamos sin tierra y algunos de nuestros compañeros se ofrecieron amablemente a bajar al patio del colegio a coger tierra... os mostramos la prueba gráfica


Seguirmos informando de nuestras avances y añadiremos alguna foto (hemos tenido problemas técnicos) en próximas entradas.
Saludos
María Alonso, Lucía García, Enol Álvarez, Pablo Pañeda y María Pumares
jueves, 12 de enero de 2012
Y aqui va la 2ª parte
Esta 2ª parte trataba de la neutralización de 50 ml de HCl y 50 ml de NaOH, gracias a la inmensa colaboración de Alvaro y Enol ya que ellos hicieron la disolución.
Al mezclarlas, y producirse por tanto la neutralizacion, aumento la temperatura de la disolución de 16.75 ºC a 22.74ºC.
Con la noticia anterior explicamos como hallar el calor total asi que nos despedimos con esta minima parte.
Un saludo.
Pañeda e Infiesta.
miércoles, 11 de enero de 2012
Hemos vuelto
La primera parte (ya que Pablo Infiesta y yo solo pudimos hacer esa parte) esta basada en una práctica de Termoquimica de la prueba PAU de quimica.
Intentamos hallar la cantidad de calor total de una disolucion de Sosa (NaOH) y agua. Al mezclarlos aumenta la temperatura de la disolución (en nuestro caso muy poco ya que para casi 100 ml de agua echamos 4g de sosa), que nos servira para hallar el calor total de la reacción a partir de esta formula:
Q=m*Ce*incremento de la temperatura
(tomaremos como Calor especifico el del agua ya que aunque sea un error, es minimo, como masa 0,1 kg , ya que tomamos como peso de las disoluciones el del agua 1g/ml, y el incremento de la temperatura que obtuvimos al medirlo con el sensor, o bien con el termometro)
La primera parte del experimento es fácil, pero nos sirve para practicar la parte practica de la PAU de quimica.
Cuando hagamos la segunda parte informaremos.
Un saludo






