Introducción:
El vinagre
es un producto natural que se obtiene del vino o la sidra por acción de unas
bacterias conocidas como Acetobacter aceti. Estos microorganismos oxidan el
etanol del vino o la sidra originales hasta convertirlo en ácido acético
(CH3-COOH). En esta práctica se pretende determinar el grado de acidez de un
vinagre, expresándolo en g/l de ácido acético.
Objetivo de la práctica:
Determinar el grado de acidez del vinagre.Fundamento teórico:
Se produce una reacción entre el ácido acético del vinagre y una disolución de hidróxido de sodio de concentración conocida. Este tipo de reacciones entre una base (hidróxido de sodio) y un ácido (acético en nuestro caso) se denominan neutralizaciones.Para conocer el momento exacto del fin de la neutralización, utilizamos un indicador de pH denominado fenolftaleína. Este pasa de incoloro (en un medio ácido) a rosa (en un medio básico).
La reacción que tendrá lugar es la siguiente: CH3-COOH + NaOH --> CH3-COONa + H2O
La
acidez se expresa en tanto por ciento en masa de ácido acético, lo que se llama
grado del vinagre.
Material y reactivos utilizados.
Materiales:
- Base y soporte.
- Nuez doble y pinzas de bureta.
- Matraz erlenmeyer de 250 mL.
- Matraz aforado de 250 mL.
- Pipeta aforada.
- Bureta de 50 mL.
Reactivos:
- Vinagre.
- Hidróxido de sodio.
- Fenoftaleína alcohólica al 0.1%
Procedimiento experimental:
- Realizamos los cálculos necesarios para realizar una disolución 0,5 M de sosa caustica.
- Con la pipeta aforada medimos 10 ml de vinagre y los vertemos en un Erlenmeyer que contenga 100 ml de agua. El agua no tiene que ser una cantidad precisa, ya que es para aumentar la superficie y poder apreciar el cambio de color de la fenolftaleína.
- Se añaden 3 o 4 gotas de fenolftaleína, el marcador de pH.
- Preparamos la bureta para recibir la disolución de sosa. La aclaramos por si quedan restos de anteriores prácticas. Cerramos la llave y la llenamos con un par de ml de sosa. Con esta cantidad procederemos a homogeneizarla, un proceso que consiste en impregnar de manera uniforme las paredes del instrumento con la sustancia en cuestión.
- Una vez realizada la homogenización descartamos esa sosa. Cargamos la bureta con una nueva cantidad de disolución y abrimos la llave para que llene también el espacio comprendido entre la misma y la pica.
- Cuando tenemos preparada la bureta, anotamos la marca en la que está situado el menisco.
- Abrimos lentamente la llave dejando caer gotas al Erlenmeyer mientras lo agitamos para asegurarnos de que los reactivos entran en contacto.
- Tras caer la primera gota que produzca un cambio de color de una duración mayor a los 30 segundos, cerramos la llave y anotamos la nueva cifra en la que este el menisco.
- Realiza los cálculos pertinentes para saber el volumen de disolución que se ha empleado en la neutralización.
- Repite el experimento para obtener otro resultado con el que hacer la media y obtener un resultado más preciso.
Cálculos y Operaciones:
·
Disolución de Sosa caustica 0,5M:
Masa Molecular Na(OH): 39,997 g/mol
· Cantidad de hidróxido de sodio gastada entre la lectura inicial y final:
1ª medida: 5.55-25.6= -20.05 (se gastaron 20.05 ml de
disolución 0,5 molar de sosa)
2ª medida: 13,2-33,2= -20 (se gastaron 20.05 ml de
disolución 0,5 molar de sosa)
Media ≈
20 ml
·
Conociendo los gramos de hidróxido de sodio
gastados, calcula cuántos gramos de ácido acético había en los 10 mL de vinagre
valorados.
Se gastaron 0,39997 gramos de sosa para neutralizar el ácido
acético. Como se trata de una neutralización 1 a 1, los gramos de sosa
utilizados serán los mismos que los gramos de ácido acético neutralizados. Por
consiguiente, en 10 ml de vinagre había 0,39997 gramos de ácido acético.
·
Sabiendo los gramos de ácido acético que hay en
10 mL de vinagre, calcula los que habrá en 100 mL.
En caso de que se pregunte los gramos de ác. Acético que
habrá en 100 ml de vinagre, serán 3,9997 gramos.
En caso de que la pregunta sea los gramos de ác. Acético
tras disolverlo en 100 ml de agua, la respuesta será: la misma cantidad ya que
lo que varía es la concentración no la cantidad de solutos.
·
Halla el grado de acidez de la muestra
analizada, es decir, los gramos de ácido acético que hay en 100 g de vinagre
(considera que la densidad del vinagre es aproximadamente la del agua d= 1 g/mL).
100 ml de vinagre≈
100 ml de vinagre
Si en 100 ml de vinagre hay 3,9997 gramos de ácido
acético, indica que su grado de acidez
es de 3,9º o 4º

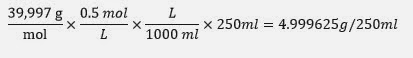


No hay comentarios:
Publicar un comentario